Combien de types de corrosion de l'aluminium existe-t-il ?
Publié le :2025-05-12 Catégorie :Le blog Vues :8047
Catalogue d'articles
Types de corrosion de l'aluminium
1. la corrosion atmosphérique
C'est la forme la plus courante de corrosion de l'aluminium. La corrosion atmosphérique de l'aluminium résulte de l'exposition aux éléments naturels. En raison de sa probabilité d'occurrence dans la plupart des endroits, la corrosion atmosphérique représente la plus grande part des dommages totaux causés à l'aluminium par tous les types de corrosion combinés dans le monde.
La corrosion atmosphérique peut être divisée en trois sous-catégories. Il s'agit de la corrosion sèche, humide et mouillée, en fonction du niveau d'humidité de l'environnement de service.
- corrosion sèche(Humidité <30%) : Seule une oxydation chimique lente se produit ;
- mouillage corrosion(Humidité 30%-60%) : corrosion galvanique localisée initiée par une fine pellicule liquide ;
- corrosion galvanique(Humidité > 60%) : un film liquide épais accélère la migration des ions et la vitesse de corrosion augmente considérablement.
Comme les niveaux d'humidité peuvent varier considérablement en fonction de l'endroit où vous vous trouvez, certaines zones connaîtront une corrosion plus importante que d'autres.
Les changements de direction du vent, la température et les précipitations sont d'autres facteurs environnementaux qui influencent l'ampleur de la corrosion atmosphérique. La concentration et le type de polluants dans l'air et la proximité de grandes étendues d'eau jouent également un rôle important.
2. la corrosion galvanique
La corrosion par couplage galvanique, également connue sous le nom de corrosion des métaux dissemblables, affecte l'aluminium lorsqu'il est physiquement ou par l'intermédiaire d'un électrolyte attaché à un métal noble. Le métal précieux peut être n'importe quel métal dont la réactivité est inférieure à celle de l'aluminium.
La réactivité d'un métal dépend de sa position dans la série électrochimique. Si un autre métal de la série électrochimique est plus éloigné de l'aluminium, la gravité de la corrosion sera plus importante.
La résistance à la corrosion est maximale à l'intersection des deux métaux et diminue à mesure que l'on s'éloigne de cette interface.
Par exemple, si de l'aluminium et du laiton sont en contact l'un avec l'autre ou même proches l'un de l'autre et placés dans de l'eau de mer, une cellule primaire se forme. La partie en aluminium se corrode alors car elle joue le rôle d'anode (borne positive).
Cela peut poser un problème dans les bateaux où les raccords en laiton peuvent se trouver à proximité de raccords en aluminium immergés dans l'eau de mer. Les électrons circulent de l'aluminium au laiton à travers l'eau de mer.
Ce type de cellule primaire peut se former par inadvertance et provoquer une corrosion par couplage galvanique dans d'autres environnements de service. La corrosion par couplage galvanique est beaucoup plus rapide que la corrosion atmosphérique normale.
- Différence de potentiel > 0,2Vs'est produite de manière significative à ce moment-là et la vitesse de corrosion était positivement corrélée avec le rapport entre la surface de la cathode et celle de l'anode ;
- Scénario type : les composants en aluminium et les raccords en laiton d'un navire traversent l'eau de mer, l'aluminium servant d'anode, et se corrodent à raison de 0,5 mm par an, soit une amélioration de 20 fois par rapport à l'état isolé ;
- Stratégie de protection : isoler les métaux dissemblables à l'aide d'entretoises isolantes ou anodiser la surface de l'aluminium.
3. piqûres

Les piqûres sont un phénomène de corrosion superficielle caractérisé par l'apparition de petits trous (piqûres) à la surface de l'aluminium. En général, ces piqûres n'affectent pas la résistance du produit. Il s'agit plutôt d'un problème esthétique, mais qui peut conduire à une défaillance si l'aspect de la surface est critique.
La corrosion par piqûres se produit généralement dans les zones où des sels sont présents dans l'atmosphère, car elle est due à la présence d'anions de chlorure. Les sulfates provoquent également, dans une certaine mesure, une corrosion par piqûres. Le pire cas de corrosion par piqûres est observé en présence de sels alcalins et acides.
condition de déclenchement: :
- Concentration d'ions chlorure (Cl-) > 0,5 mol/L ;
- La présence d'inclusions ou de défauts des joints de grains à la surface ;
- Le potentiel de l'alliage est plus élevé que le potentiel de claquage local (>0,4V par rapport au SCE).
Mécanisme d'extension: : - L'hydrolyse de l'Al³⁺ dans le pore de gravure produit de l'acide (pH jusqu'à 2-3) et l'enrichissement en Cl- forme un cycle autocatalytique ;
- Le taux de croissance de la profondeur du trou peut atteindre 0,1 mm/mois, et le rapport profondeur/largeur est souvent >10:1.
Pour qu'il y ait piqûre, le potentiel de l'alliage doit être supérieur au potentiel de l'électrolyte (solution saline). La présence de défauts de surface aux joints de grains et de particules de seconde phase est un précurseur de piqûres.
4. la corrosion caverneuse
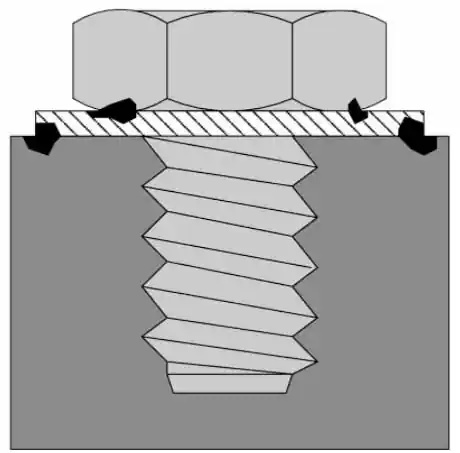
La corrosion caverneuse est une forme de corrosion localisée dans les matériaux. Des matériaux qui se chevauchent ou des erreurs de conception involontaires peuvent entraîner la formation de crevasses. Par conséquent, l'accumulation d'eau de mer dans ces poches peut entraîner une corrosion caverneuse.
Il suffit d'un petit espace entre le boulon et la structure pour déclencher ce type de corrosion. Avec le temps, l'aluminium contenu dans le matériau se dissout et se précipite dans l'eau de mer. Cet aluminium ionique absorbe l'oxygène de l'air ambiant et les ions hydroxyde de l'électrolyte pour former de l'hydroxyde d'aluminium.
Les zones géométriquement restreintes (par exemple, les joints de bride, les espaces entre les rivets) forment des cellules d'occlusion en raison des différences de diffusion de l'oxygène :
- phase initialeLa dissolution de l'aluminium est due à la différence de concentration d'oxygène à l'intérieur et à l'extérieur de la fente (Al→Al³⁺+3e-) ;
- période de développement: L'hydrolyse de l'Al³⁺ entraîne une diminution du pH et une migration du Cl- vers la concentration ;
- plateauL'eau de Javel : maintient un microenvironnement fortement corrosif à un pH ≈ 2, avec le plus grand risque à une largeur d'espace de 0,1-0,5 mm.
En présence de chlorures, cette réduction de l'oxygène rend les crevasses acides, ce qui accélère la vitesse de corrosion.
5. la corrosion intergranulaire
Pour l'aluminium, les joints de grains sont électrochimiquement différents de la microstructure de l'alliage. Cela conduit à l'établissement d'un potentiel électrochimique et à l'échange d'électrons entre les deux.
Il existe plusieurs variantes de la corrosion intergranulaire en fonction du traitement thermochimique et de la structure du métal. Elle est également présente à des degrés divers dans les différentes séries d'alliages d'aluminium. Par exemple, les alliages de la série 6xxx sont relativement insensibles à ce type de corrosion de l'aluminium.
La trajectoire de l'anode varie selon les systèmes d'alliage. Dans la série 2xxx, il se présente comme une bande étroite de part et d'autre du joint de grain, tandis que dans la série 5xxx, il se présente comme un chemin continu le long du joint de grain.
Le phénomène de dissolution préférentielle le long des joints de grains provient de l'hétérogénéité des tissus :
- Département de 2xxxLa précipitation de CuAl₂ aux joints de grains conduit à une zone pauvre en cuivre (anode) ;
- Département de 5xxx: Traitement sélectif déclenché par une phase β continue (Mg₂Al₃) ;
- protégerLe traitement de vieillissement T6 réduit la profondeur de la corrosion des joints de grains par 80%.
Comme la piqûre, la corrosion intergranulaire commence par une piqûre. Cependant, elle se propage plus rapidement le long des joints de grains sensibles.
6. corrosion par écaillage
La corrosion par écaillage est un type spécifique de corrosion intergranulaire que l'on trouve dans les alliages d'aluminium à structure orientée prononcée. Elle est particulièrement évidente dans les produits en aluminium qui ont été soumis à un processus de laminage à chaud ou à froid.
Elle se produit le long des joints de grains allongés dans la microstructure. Le terme écaillage vient du fait que les produits de corrosion sont beaucoup plus gros et donnent l'impression de se détacher de la surface du matériau.
Ce type de corrosion de l'aluminium s'étend au-delà de la surface et crée des tensions latérales dans le produit. Il en résulte une action initiale de coincement à la surface avant de migrer dans le corps du produit. Une délamination importante se produit et le matériau s'affaiblit. Une dégradation de la surface telle que des piqûres, des écaillages et des boursouflures peut se produire.
Les séries 2xxx, 5xxx et 7xxx sont plus sensibles à la corrosion par exfoliation en raison de leur structure de grain fortement orientée. Cela rend les joints de grains plus sensibles à la corrosion intergranulaire. Corrosion laminaire dans les tôles laminées en raison d'une organisation anisotrope :
Le test accéléré de la solution EXCO pendant 48h simule le niveau de corrosion naturel pendant 10 ans.
L'expansion du volume des produits de corrosion (Al → Al(OH)₃ augmentation du volume d'un facteur de 6,3) déclenche des contraintes entre les couches (>100 MPa) dans le sens du laminage parallèle ;
La susceptibilité à la corrosion par exfoliation peut être modifiée en redistribuant les précipités à l'aide de méthodes de traitement thermique.
7. corrosion générale
Lorsque la corrosion se produit presque uniformément sur la surface d'un produit en aluminium, il s'agit d'une corrosion uniforme ou totale.
Cette corrosion se produit lorsque les produits sont fréquemment exposés à des milieux fortement acides ou alcalins. Elle peut également se produire en présence de potentiels électrochimiques élevés lorsque le produit se trouve dans un électrolyte. Un exemple typique est la rouille des tôles d'aluminium dans les solutions acides.
La corrosion uniforme est le résultat d'un mouvement continu des régions de l'anode et de la cathode en contact avec l'électrolyte et se manifeste par une attaque corrosive uniforme sur la surface.
La couche d'oxyde est également instable dans les solutions à pH élevé ou faible et ne protège pas le métal sous-jacent. L'épaisseur du matériau diminue et finit par se dissoudre complètement.
Les attaques ne sont pas tout à fait cohérentes et il y a des pics et des creux. Il n'y a pas de petites zones de corrosion profonde suffisantes pour que l'on puisse parler d'un exemple général de corrosion.
Le film de passivation est complètement dissous dans des environnements fortement acides (pH 9) :
- taux de corrosion>1,2 mm/an à pH 9 ;
- L'acide nitrique concentré (65%) réduit le taux à 0,001 mm/an en raison d'une forte passivation.
8. corrosion par dépôt
La corrosion par dépôt se produit lorsque des métaux différents se déposent sur une surface d'aluminium, ce qui entraîne une corrosion localisée importante.
Imaginez que de l'eau s'écoule dans un tuyau en cuivre. Au fur et à mesure que l'eau s'écoule, elle absorbe des ions de cuivre. Ces ions de cuivre sont maintenant en solution. Lorsque cette solution entre en contact avec une surface ou un récipient en aluminium, elle y dépose ces ions de cuivre.
Ces ions forment maintenant une protocellule subtile et si l'ion est bas dans la série électrochimique ou protocellulaire, il corrodera l'aluminium par piqûres. Plus la différence entre l'aluminium et les ions déposés couplés électriquement est importante, plus la corrosion est grave.
Même des solutions d'ions cuivre à une concentration de 1 ppm sont connues pour provoquer une grave corrosion des surfaces en aluminium.
Les métaux susceptibles de provoquer la corrosion des dépôts d'aluminium sont appelés "métaux lourds". Certains métaux lourds importants sont le cuivre, le mercure, l'étain, le nickel et le plomb.
Le film de passivation est complètement dissous dans des environnements fortement acides (pH 9) :
- taux de corrosion>1,2 mm/an à pH 9 ;
- L'acide nitrique concentré (65%) réduit le taux à 0,001 mm/an en raison d'une forte passivation.
La corrosion causée par cette méthode est plus prononcée dans les solutions acides que dans les solutions alcalines. Ceci est dû à la faible solubilité de ces ions dans les solutions alcalines.
9. la corrosion sous contrainte (SCC)

La corrosion sous contrainte (appelée ici CSC) est une forme de corrosion intergranulaire qui peut entraîner la défaillance complète des pièces en aluminium.
Trois conditions doivent être réunies pour que cette corrosion se produise. Les alliages sensibles sont les premiers concernés. Tous les alliages d'aluminium ne sont pas également sensibles à la CSC. Les alliages à haute limite d'élasticité sont plus sensibles à la corrosion fissurante sous contrainte.
La deuxième condition est que l'environnement dans lequel il est utilisé soit humide ou mouillé. La troisième condition est la présence d'une contrainte de traction dans le matériau. Cette contrainte de traction est à l'origine de la propagation des fissures et de leur propagation à travers le métal.
triptyqueAlliages sensibles (par exemple 7075-T6), contraintes de traction (> limite d'élasticité 30%), milieux corrosifs (solution de Cl) :
- Type de fissureLes deux types d'échantillons sont : le long du grain (IGSCC) ou à travers le grain (TGSCC) ;
- Le facteur d'intensité de contrainte critique (KISCC) peut être réduit à 30% de la résistance conventionnelle.
Il existe deux types de processus de CSC. Le premier est la fissuration intergranulaire par corrosion sous contrainte (IGSCC), dans laquelle les fissures se propagent le long des joints de grains. La seconde est la fissuration par corrosion sous contrainte à travers les grains (TGSCC), dans laquelle les fissures se propagent à travers les grains plutôt que le long des joints de grains.
10. érosion corrosion

La corrosion par érosion de l'aluminium est causée par l'impact de jets d'eau à grande vitesse sur le corps en aluminium.
Deux facteurs exacerbent l'érosion-corrosion : le débit de l'eau et son pH. La présence de carbonate et de silice dans l'eau augmente encore la vitesse de corrosion.
Dans l'eau pure, la corrosion de l'aluminium est lente. Toutefois, cette vitesse augmente lorsque le pH dépasse 9. Dans l'eau acide, la corrosion est encore plus rapide.
Dynamique des fluides et corrosion chimique en synergie :
- vitesse élevée(>5m/s) détruit le film de passivation ;
- un fluide sablonneuxDommages provoqués par l'interaction abrasion-corrosion ;
- effondrement de la vacuoleGénère une pression d'impact >1GPa entraînant un écaillage de la surface.
L'érosion-corrosion peut être évitée en contrôlant les facteurs ci-dessus. L'érosion-corrosion peut être réduite de manière significative en réduisant la vitesse de l'eau, en maintenant la qualité de l'eau, ou les deux. L'amélioration de la qualité de l'eau consiste à maintenir le pH aussi proche que possible de la neutralité (<9) et à réduire les niveaux de silice et de carbonate.
11. fatigue due à la corrosion
Il est bien connu que la fatigue peut conduire à une défaillance complète du produit si elle n'est pas contrôlée. Dans le cas de l'aluminium, la fissuration par fatigue peut servir de point de départ à la corrosion par piqûres.
La fatigue due à la corrosion se produit lorsque l'aluminium est soumis de manière répétée à de faibles contraintes sur une longue période. Dans les environnements corrosifs tels que l'eau de mer et les solutions salines, l'apparition et l'expansion de fissures sont plus susceptibles de se produire.
Réduction synergique de la limite de fatigue par l'alternance de charges et de milieux corrosifs :
- 3.5% solution NaCl, la durée de vie en fatigue de l'alliage d'aluminium 2024-T3 est réduite à 10% dans un environnement sec ;
- La vitesse d'extension des fissures est régulée par ΔK (amplitude du facteur d'intensité des contraintes) et la fréquence (seuil critique de 10 Hz).
La fatigue par corrosion ne peut se produire si l'eau n'est pas présente dans l'atmosphère. Elle est également largement indépendante de la direction de la contrainte, puisque la propagation des fissures se fait principalement à travers le cristal. Ainsi, contrairement à la CSC, la contrainte n'affecte pas sa propagation.
12. corrosion filamenteuse

La corrosion filamentaire ou vermiforme commence par des piqûres. Elle commence à l'endroit où la peinture se détache de la surface de l'aluminium. La cause peut être une rayure ou une abrasion de la surface qui expose la surface métallique sous-jacente.
En présence d'anions chlorure et d'une humidité élevée, la corrosion filiforme peut facilement apparaître et se propager. Bien qu'elle commence par des piqûres de corrosion dues à l'eau salée, elle se propage sous la forme d'une corrosion en creux.
La tête du ver de terre est acide et contient beaucoup de chlorure. Elle absorbe l'oxygène et agit comme une anode. La seconde moitié de la piste du ver agit comme une cathode et une réaction s'ensuit.
La corrosion autopropulsée s'est formée au niveau des défauts du revêtement :
- La zone acide de la tête (pH ≈ 1-2) et la zone alcaline de la queue (pH ≈ 10-12) forment un gradient électrochimique ;
- Taux d'extension de 0,1 à 0,5 mm/jour, trajectoire contrôlée par la trame de la matrice.
La corrosion filamenteuse peut être évitée en maintenant la surface intacte et en colmatant toutes les petites fentes avec de la peinture ou de la cire. Si possible, l'humidité relative de l'environnement doit être réduite.
13. corrosion microbiologique(MIC)
La corrosion microbiologiquement induite (MIC) est une corrosion causée par des micro-organismes/champignons. Ce type de corrosion est courant dans les réservoirs de carburant et d'huile de graissage.
Les micro-organismes et les champignons peuvent se développer en présence d'eau dans l'huile. Certains de ces organismes sont capables de consommer l'huile et d'excréter des acides qui peuvent provoquer la corrosion des conteneurs en aluminium utilisés pour le stockage.
Cet acide peut provoquer des piqûres dans les conteneurs en aluminium et éventuellement entraîner des fuites.
déclenché par le métabolisme microbien tel que les bactéries réduisant les sulfates (SRB) :
- L'environnement anaérobie produit du H₂S qui détruit le film de passivation ;
- Les biofilms forment des cellules de concentration d'oxygène ;
- La zone de séparation de la phase aqueuse du système d'alimentation en carburant est une zone à forte incidence qui nécessite une vidange régulière et l'ajout d'un biocide.
Pour éviter cela, l'huile doit être purifiée autant que possible pour éliminer l'eau. Une vidange régulière du réservoir après la purification est également nécessaire. S'il n'est pas possible d'améliorer la qualité du carburant, il est possible d'empêcher la germination en utilisant des biocides.


























